中國醫(yī)藥化工網(wǎng)3月28日訊 盡管生物類似藥目前的市場規(guī)模并不算大,只有區(qū)區(qū)幾十億美元,卻“熱”得燙手。
國內(nèi)外許多藥企都已經(jīng)或打算進軍生物類似藥市場,世界著名仿制藥公司如梯瓦(以色列)、山德士(瑞士,諾華旗下)等均加大了對生物類似藥的投資力度,更有不少世界原研制藥巨頭如輝瑞(美國)、默沙東(美國)、安進(美國)、勃林格殷格翰(德國)等也紛紛進軍生物類似藥。
熱潮涌動的推手
生物類似藥火熱的背后原因和驅(qū)動因素,筆者認為有3個:一是日益升高的新藥開發(fā)成本,二是到期的生物藥專利,三是市場對生物藥的巨大需求。
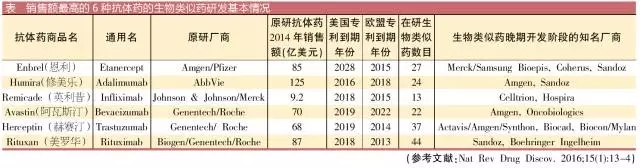
下表是銷售額最高的6種抗體藥(包括Fc融合蛋白Enbrel)。其中,對專利部分的內(nèi)容因數(shù)據(jù)已經(jīng)過時,所以進行了簡單更新。“藥王”Humira(修美樂)在2014年的全球銷售額是125億美元,2015年更是漲到了146億美元,因此在研生物類似藥多達24個就不足為奇了。Rituxan(美羅華)的在研生物類似藥更是多達44個。

毫無疑問,這么多廠家扎堆少數(shù)幾個銷售額最高的藥,笑到最后的只能是“一小撮”贏家。
六個主要挑戰(zhàn)
盡管目前看來生物類似藥的前(錢)景不錯,但其未來也面臨許多挑戰(zhàn)和風(fēng)險,值得已經(jīng)或?qū)⒁M入這個領(lǐng)域的企業(yè)重視。面對火熱的生物類似藥需要冷靜思考,多考慮一些潛在的投資風(fēng)險。
筆者認為,生物類似藥的主要挑戰(zhàn)至少有如下6點:
1.與化學(xué)藥相比,生物類似藥的價格沒有太多優(yōu)勢,生物藥的特點決定其開發(fā)和生產(chǎn)成本要遠高于化學(xué)仿制藥。與原研生物藥相比,其降價空間非常有限,盡管已經(jīng)有報道,在印度和北歐有的生物類似藥的價格可以低至原研藥的2~3成,但這樣的低價很難持久。在監(jiān)管嚴格(也意味著成本更高)的歐美主流市場更是很難采用低價策略占領(lǐng)市場。一般認為,將來在美國市場上銷售的生物類似藥,其價格只會比原研藥低20%~30%。
2.美國生物類似藥的市場前景并不是很樂觀。盡管有些知名機構(gòu)預(yù)測,到2020年生物類似藥的全球銷售額會超過100億美元,但無論這個數(shù)字多么誘人,是否最終能達到預(yù)測值很大程度上取決于全球最大的市場美國的情況,而這又很大程度上取決于FDA對生物類似藥的政策。
正如筆者在這個系列的上一篇文章“生物仿制藥VS.化學(xué)仿制藥”(點擊閱讀)中所提到的,F(xiàn)DA已經(jīng)將普通的生物類似藥認定為不可自動替換(non-interchangeable),這顯然是生物類似藥一個很大的障礙??梢灶A(yù)見,可自動替換的生物類似藥短期內(nèi)很難獲得FDA的上市批準(zhǔn)。
3.讓醫(yī)生接受生物類似藥需要時間。最近的一個美國的調(diào)查顯示:只有一半的美國醫(yī)生在未來三年內(nèi)會考慮向病人開出生物類似藥處方。
4.生物原研藥廠家會想方設(shè)法阻礙生物類似藥進入市場。最近艾伯維(Abbvie)和安進(Amgen)有關(guān)Humira(修美樂)和安進的生物類似藥的專利之戰(zhàn)就是一個例子。被仿制的原研生物藥都是各大公司的“搖錢樹”,當(dāng)然不會坐以待斃,會采用多種措施阻礙生物類似藥蠶食自己的市場。
5.與原研生物藥廠家相比,絕大多數(shù)生物類似藥企業(yè)在主要的關(guān)鍵治療領(lǐng)域(如癌癥和免疫疾?。┒夹枰鰪娚镱愃扑幍拈_發(fā)和生產(chǎn)能力,而這都需要時間。
6.原研藥廠家憑借在關(guān)鍵治療領(lǐng)域的優(yōu)勢,繼續(xù)開發(fā)其重磅產(chǎn)品的“me-better”,以便進一步狙擊潛在的“生物類似藥競爭者”的市場蠶食。 (本報特約 美中藥源專欄)



 110102000668(1)號
110102000668(1)號