醫(yī)藥網(wǎng)7月30日訊 7月29日,上海陽光醫(yī)藥采購網(wǎng)發(fā)布“國家組織藥品集中采購和使用聯(lián)合采購辦公室關(guān)于發(fā)布《全國藥品集中采購文件(GY-YD2020-1)》的公告(國聯(lián)采字〔2020〕1號(hào))”,同時(shí)掛網(wǎng)公布《采購品種目錄》《各地首年約定采購量》和《各采購品種首年約定采購量》。
《全國藥品集中采購文件(GY-YD2020-1)》(以下稱《文件》)指出,本次采購品種目錄中同品種最多入圍企業(yè)數(shù)根據(jù)符合“申報(bào)品種資格”的實(shí)際申報(bào)企業(yè)數(shù)確定,最多8家。申報(bào)信息公開、供應(yīng)地區(qū)確認(rèn)時(shí)間和地點(diǎn)為2020年8月20日(星期四)上午10點(diǎn),上海市長寧區(qū)虹橋路2419號(hào)龍柏飯店云廷會(huì)場。
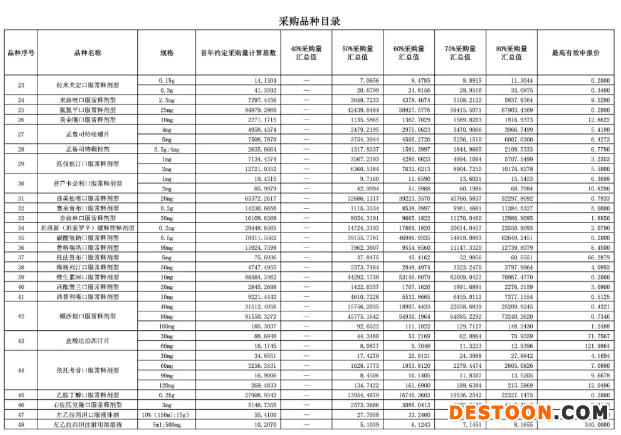
注射劑采購周期僅一年
《文件》指出,本次藥品集中采購周期自中選結(jié)果實(shí)際執(zhí)行日起,以年為單位。各地首年約定采購量計(jì)算基數(shù)由各地確定。各地首年約定采購量及各采購品種首年約定采購量。
各品種各地首年約定采購量按以下規(guī)則確定:
全國實(shí)際中選企業(yè)數(shù)為1家的,為首年約定采購量計(jì)算基數(shù)的50%;
全國實(shí)際中選企業(yè)數(shù)為2家的,為首年約定采購量計(jì)算基數(shù)的60%;
全國實(shí)際中選企業(yè)數(shù)為3家的,為首年約定采購量計(jì)算基數(shù)的70%;
全國實(shí)際中選企業(yè)數(shù)為4家及以上的,為首年約定采購量計(jì)算基數(shù)的80%。
其中阿莫西林顆粒劑、利奈唑胺口服常釋劑型、莫西沙星氯化鈉注射劑、左氧氟沙星滴眼劑、環(huán)丙沙星口服常釋劑型、頭孢地尼口服常釋劑型、頭孢克洛口服常釋劑型、克拉霉素口服常釋劑型各地首年約定采購量按以下規(guī)則確定:
全國實(shí)際中選企業(yè)數(shù)為1家的,為首年約定采購量計(jì)算基數(shù)的40%;
全國實(shí)際中選企業(yè)數(shù)為2家的,為首年約定采購量計(jì)算基數(shù)的50%;
全國實(shí)際中選企業(yè)數(shù)為3家的,為首年約定采購量計(jì)算基數(shù)的60%;
全國實(shí)際中選企業(yè)數(shù)為4家及以上的,為首年約定采購量計(jì)算基數(shù)的70%。
關(guān)于采購周期,《文件》指出各品種各地采購周期按以下規(guī)則確定:
全國實(shí)際中選企業(yè)數(shù)為1家或2家的,本輪采購周期原則上為1年;
全國實(shí)際中選企業(yè)數(shù)為3家的,本輪采購周期原則上為2年;
全國實(shí)際中選企業(yè)數(shù)為4家及以上的,本輪采購周期原則上為3年。
其中阿扎胞苷注射劑、莫西沙星氯化鈉注射劑、左乙拉西坦注射用濃溶液本輪采購周期原則上為1年。
采購周期內(nèi)采購協(xié)議每年一簽。續(xù)簽采購協(xié)議時(shí),約定采購量原則上不少于各地該中選藥品上年約定采購量。采購周期內(nèi)若提前完成當(dāng)年約定采購量,超出部分中選企業(yè)仍按中選價(jià)進(jìn)行供應(yīng),直至采購周期屆滿。
將于三周后開標(biāo)
《文件》明確,申報(bào)企業(yè)資格為提供藥品及伴隨服務(wù)的國內(nèi)藥品生產(chǎn)企業(yè)、藥品上市許可持有人、藥品上市許可持有人(為境外企業(yè))指定的進(jìn)口藥品全國總代理。符合申報(bào)要求的企業(yè)須在規(guī)定時(shí)間提交申報(bào)材料,未提交的,將影響該企業(yè)所涉藥品在全國范圍內(nèi)的集中采購活動(dòng)。
屬于采購品種目錄范圍并獲得國內(nèi)有效注冊批件的上市藥品,且滿足以下要求之一的將獲得申報(bào)品種資格:1.原研藥及國家藥品監(jiān)督管理局發(fā)布的仿制藥質(zhì)量和療效一致性評價(jià)參比制劑;2.通過國家藥品監(jiān)督管理局仿制藥質(zhì)量和療效一致性評價(jià)的仿制藥品;3.根據(jù)《國家食品藥品監(jiān)督管理總局關(guān)于發(fā)布化學(xué)藥品注冊分類改革工作方案的公告》〔2016年第51號(hào)〕,按化學(xué)藥品新注冊分類批準(zhǔn)的仿制藥品;4.納入《中國上市藥品目錄集》的藥品。
《文件》另外指出,申報(bào)企業(yè)須確保在采購周期內(nèi)滿足供應(yīng)地區(qū)中選藥品約定采購量需求;供應(yīng)品種清單應(yīng)包含采購品種目錄內(nèi)本企業(yè)生產(chǎn)的所有符合“申報(bào)品種資格”的規(guī)格;應(yīng)遵守《專利法》《反不正當(dāng)競爭法》等相關(guān)法律法規(guī),并承擔(dān)相應(yīng)法律責(zé)任;申報(bào)藥品應(yīng)當(dāng)符合國家藥品標(biāo)準(zhǔn)和經(jīng)國家藥品監(jiān)督管理部門核準(zhǔn)的藥品質(zhì)量標(biāo)準(zhǔn),并按照國家藥監(jiān)局藥審中心關(guān)于發(fā)布《化學(xué)藥物中亞硝胺類雜質(zhì)研究技術(shù)指導(dǎo)原則(試行)》的通告(2020年1號(hào))組織生產(chǎn)。
聯(lián)合采購辦公室將于8月20日(星期四)上午7點(diǎn)30分在上海市長寧區(qū)虹橋路2419號(hào)龍柏飯店牡丹廳會(huì)場開始接收申報(bào)材料,遞交截止時(shí)間為同日上午10點(diǎn)。10點(diǎn)后將公開申報(bào)信息,供應(yīng)地區(qū)確認(rèn)時(shí)間為同日下午2點(diǎn)。
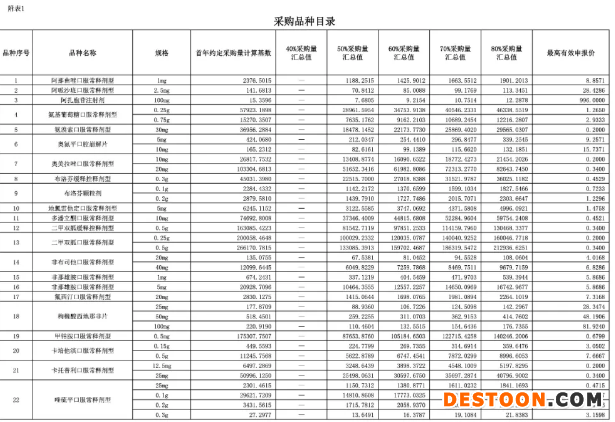
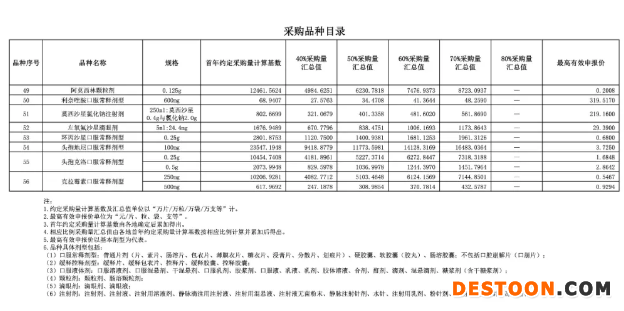
采購品種目錄

來源:醫(yī)藥網(wǎng)



 110102000668(1)號(hào)
110102000668(1)號(hào)