8月13日訊 8月11日,河北省藥監(jiān)局官網(wǎng)發(fā)布《關(guān)于推進(jìn)藥品流通追溯系統(tǒng)中藥飲片追溯工作的通知》(下稱《通知》),將一批中藥飲片納入藥品流通追溯系統(tǒng),并選定20家藥品批發(fā)企業(yè)進(jìn)行中藥飲片標(biāo)準(zhǔn)數(shù)據(jù)對(duì)照和追溯數(shù)據(jù)上傳工作。
飲片追溯“河北方案”
河北此次第一批納入藥品流通追溯系統(tǒng)的中藥飲片主要包括執(zhí)行《中國(guó)藥典》、《衛(wèi)生部藥品標(biāo)準(zhǔn)》中藥材第一冊(cè)、《河北省中藥飲片炮制規(guī)范》2003年版、《河北省中藥材標(biāo)準(zhǔn)》2018年版的中藥飲片品種,以及涉及批發(fā)企業(yè)經(jīng)營(yíng)的其他中藥飲片品種。
值得注意是的,河北省此次選定了20家藥品批發(fā)企業(yè)(見下表)進(jìn)行中藥飲片標(biāo)準(zhǔn)數(shù)據(jù)對(duì)照和追溯數(shù)據(jù)上傳工作。要求企業(yè)按照中藥飲片名稱、執(zhí)行標(biāo)準(zhǔn)、生產(chǎn)企業(yè)、產(chǎn)地等產(chǎn)品信息,對(duì)照《中藥飲片基礎(chǔ)數(shù)據(jù)標(biāo)準(zhǔn)化對(duì)照表(第一批)》,形成品種編碼對(duì)應(yīng)關(guān)系。將本單位中藥飲片的供貨商、客戶的所屬區(qū)域與中心的“行政區(qū)域信息”進(jìn)行對(duì)照,形成區(qū)域代碼對(duì)應(yīng)關(guān)系。
表 第一批加入河北省中藥飲片追溯企業(yè)名單
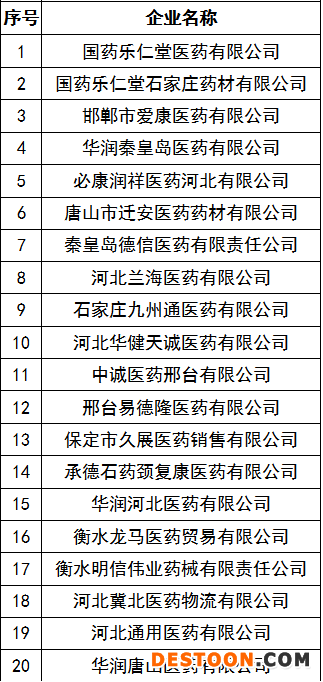
按照《通知》要求,上述20家批發(fā)企業(yè)需要在所有品種對(duì)照完成后,生成本企業(yè)中藥飲片進(jìn)銷存XML數(shù)據(jù)文件,按照原藥品制劑進(jìn)銷存XML數(shù)據(jù)上傳方式,每日向系統(tǒng)上傳。在2020年8月12日完成中藥飲片品種對(duì)照和追溯數(shù)據(jù)上傳工作。
有行業(yè)人士指出,河北此次以批發(fā)企業(yè)作為中藥飲片追溯抓手并不意外,去年該省就已發(fā)文要求全省藥品批發(fā)企業(yè)和零售連鎖企業(yè)須在9月15日前全部加入河北省藥品追溯系統(tǒng)。“當(dāng)時(shí)的文件就指出,藥品追溯系統(tǒng)首先將實(shí)施批準(zhǔn)文號(hào)和注冊(cè)證號(hào)管理(進(jìn)口藥品)的藥品納入監(jiān)控范圍,將中藥飲片納入監(jiān)控范圍已在后續(xù)計(jì)劃中。而入網(wǎng)后藥品經(jīng)營(yíng)企業(yè)每日上報(bào)藥品進(jìn)銷存信息情況也是在去年文件中已經(jīng)明確,此次只是把中藥飲片也納入。”
全產(chǎn)業(yè)鏈監(jiān)管仍待加強(qiáng)
中藥飲片的整治可以說(shuō)是近年監(jiān)管的重點(diǎn)之一。在年初的全國(guó)藥品注冊(cè)管理工作和上市后監(jiān)管工作會(huì)議上,也提出要聚焦藥品安全難點(diǎn)領(lǐng)域、突出問題,深入開展中藥飲片、執(zhí)業(yè)藥師“掛證”等專項(xiàng)整治。
其實(shí),近年隨著監(jiān)管工作的加強(qiáng)、行業(yè)質(zhì)量意識(shí)的提升,國(guó)內(nèi)中藥材及中藥飲片的質(zhì)量逐年好轉(zhuǎn)。數(shù)據(jù)顯示,去年全國(guó)抽驗(yàn)的54188批中藥材及飲片質(zhì)量檢驗(yàn),平均合格率已達(dá)到91%,總體質(zhì)量情況呈現(xiàn)穩(wěn)中向好的趨勢(shì)。
2013-2019年全國(guó)中藥材及飲片抽驗(yàn)合格率
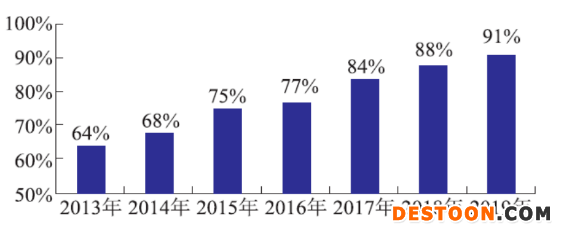
(來(lái)源:中國(guó)食品藥品檢定研究院)
中藥飲片和制劑生產(chǎn)經(jīng)營(yíng)使用單位以及中藥材市場(chǎng)要落實(shí)好主體責(zé)任,尤其是作為源頭的生產(chǎn)企業(yè)。《藥品管理法》第三十九條規(guī)定,中藥飲片生產(chǎn)企業(yè)履行藥品上市許可持有人的相關(guān)義務(wù),對(duì)中藥飲片生產(chǎn)、銷售實(shí)行全過(guò)程管理,建立中藥飲片追溯體系,保證中藥飲片安全、有效、可追溯。
目前,對(duì)于中藥飲片的抽檢主要在銷售和使用環(huán)節(jié)抽樣。按照有關(guān)規(guī)定,抽檢的中藥飲片若經(jīng)檢驗(yàn)不符合標(biāo)準(zhǔn)規(guī)定或檢出非法成分,標(biāo)示生產(chǎn)企業(yè)所在地藥監(jiān)部門按規(guī)定送達(dá)檢驗(yàn)報(bào)告書和“擬公告告知書”時(shí),需由標(biāo)示生產(chǎn)企業(yè)在送達(dá)回執(zhí)中書面確認(rèn)是否生產(chǎn)過(guò)涉及的不合格產(chǎn)品,以便采取相應(yīng)的監(jiān)管措施。
《醫(yī)藥經(jīng)濟(jì)報(bào)》記者檢索了2020年在國(guó)家藥監(jiān)局網(wǎng)站發(fā)布的2020年各地監(jiān)管信息,涉及不合格中藥飲片的有14期,共計(jì)123個(gè)批次不合格中藥飲片,其中有23個(gè)批次的標(biāo)示生產(chǎn)企業(yè)否認(rèn)生產(chǎn),占18.7%。可見,不合格中藥飲片標(biāo)示生產(chǎn)企業(yè)否認(rèn)生產(chǎn)的情況依然存在。
分析人士認(rèn)為,中藥飲片追溯的完善、追溯體系的健全可以大大減低類似的情況的發(fā)生,如此次把中藥飲片納入監(jiān)控范圍的河北藥品追溯系統(tǒng),就對(duì)第一批入網(wǎng)的藥品批發(fā)企業(yè)及視頻傳輸條件成熟企業(yè)試行視頻傳輸非現(xiàn)場(chǎng)監(jiān)控,將企業(yè)倉(cāng)庫(kù)視頻監(jiān)控接入藥品流通非現(xiàn)場(chǎng)監(jiān)控系統(tǒng),藥品監(jiān)管部門可實(shí)時(shí)查看藥品經(jīng)營(yíng)企業(yè)倉(cāng)庫(kù)視頻監(jiān)控。
此外,物聯(lián)網(wǎng)、條形碼、射頻識(shí)別(RFID)、大數(shù)據(jù)等技術(shù)的應(yīng)用,也有望強(qiáng)化從流通鏈條上對(duì)中藥飲片質(zhì)量的保障。



 110102000668(1)號(hào)
110102000668(1)號(hào)