50條負面清單發(fā)布
近日,山東省藥品監(jiān)督管理局發(fā)布《醫(yī)療器械經(jīng)營企業(yè)、使用單位質(zhì)量安全主體責任清單和負面清單的通知》(以下簡稱《通知》)。
《通知》稱,山東省藥監(jiān)局依據(jù)《醫(yī)療器械監(jiān)督管理條例》《醫(yī)療器械經(jīng)營監(jiān)督管理辦法》《醫(yī)療器械使用質(zhì)量監(jiān)督管理辦法》等,研究制定了醫(yī)療器械經(jīng)營企業(yè)、使用單位質(zhì)量安全主體責任清單和負面清單。
具體如下:
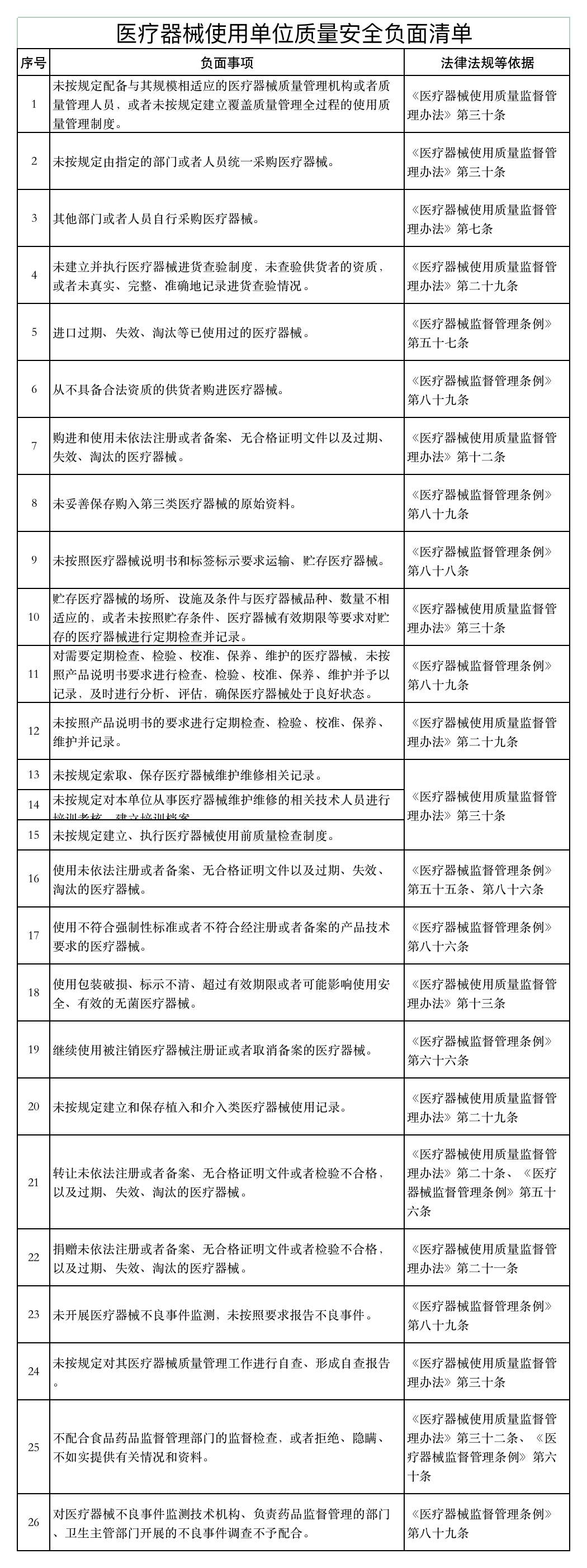
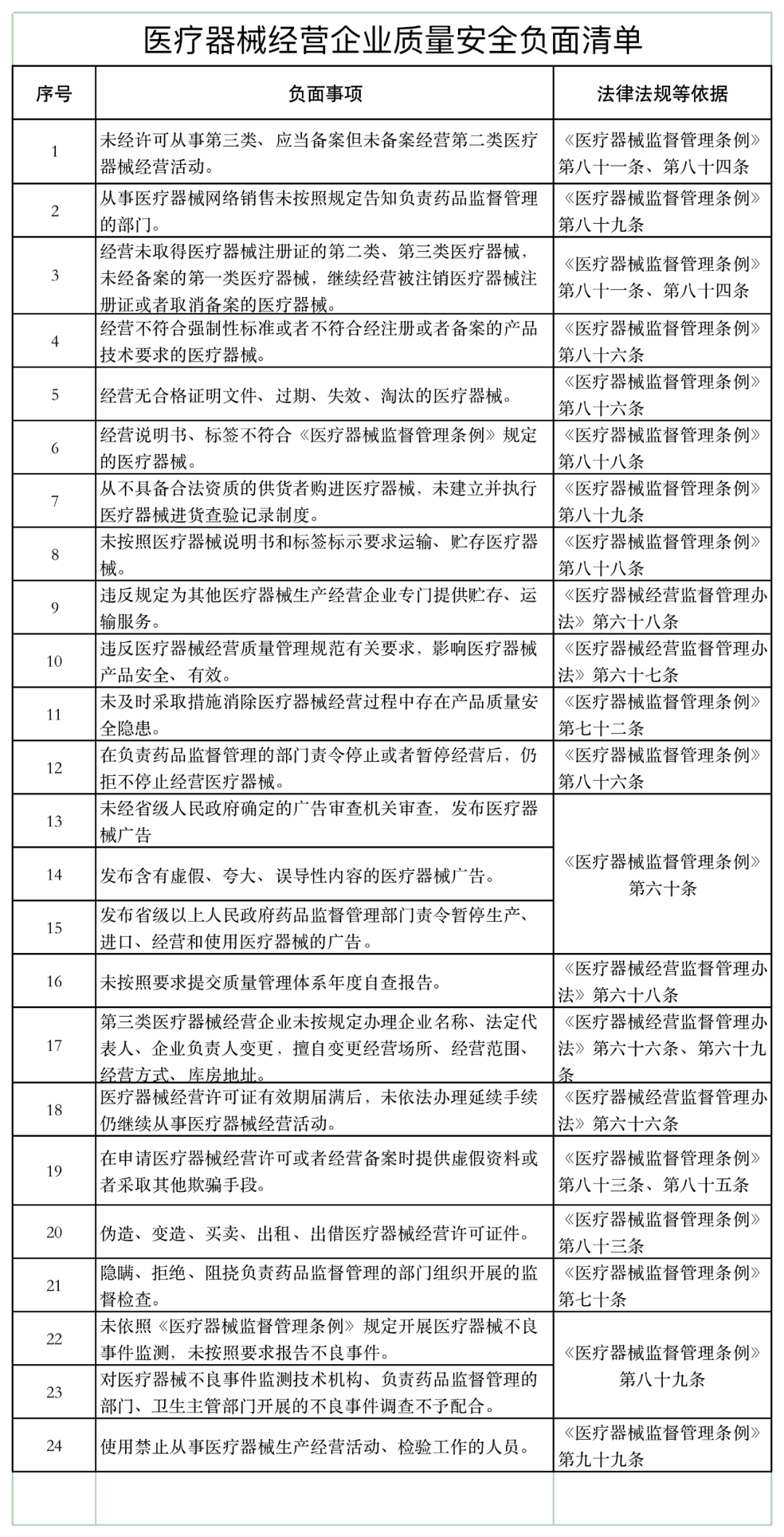
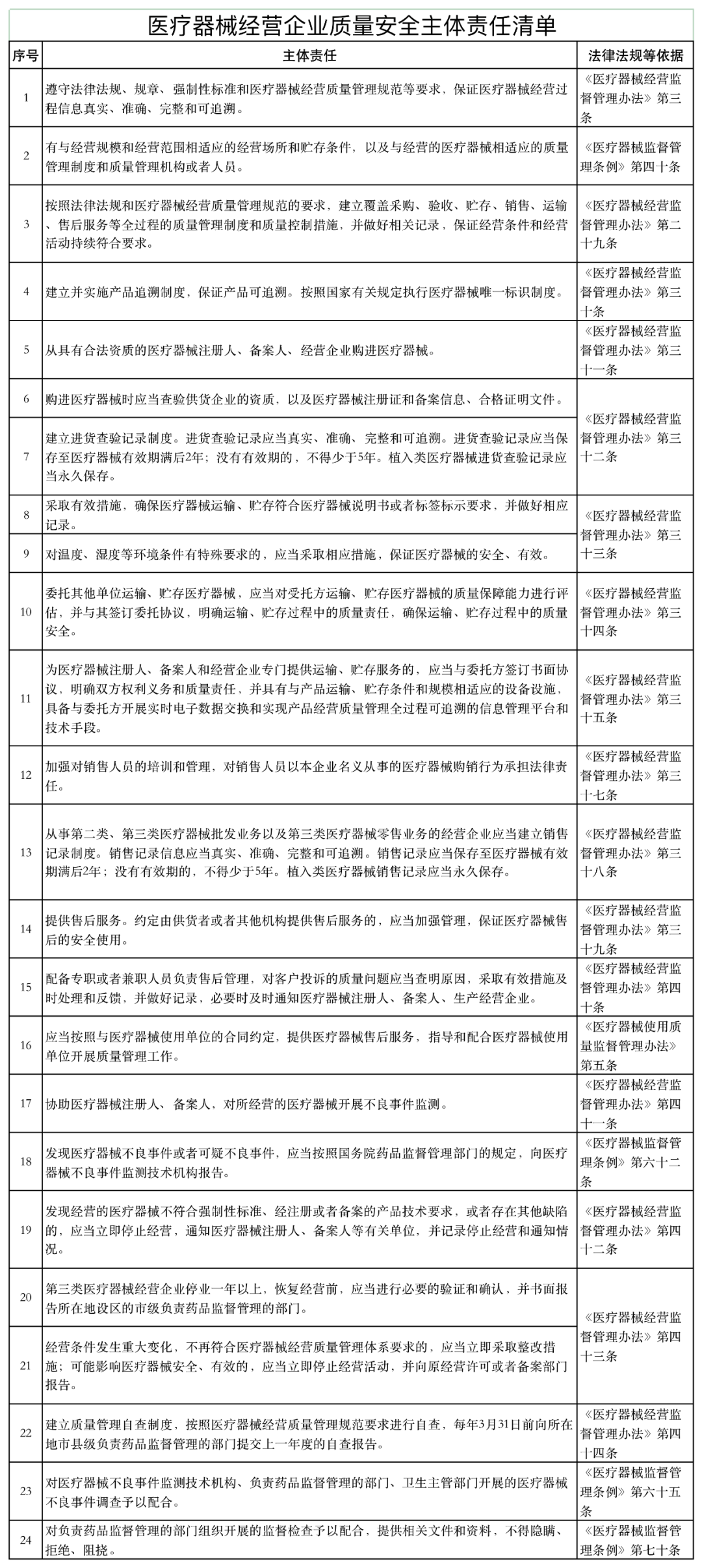
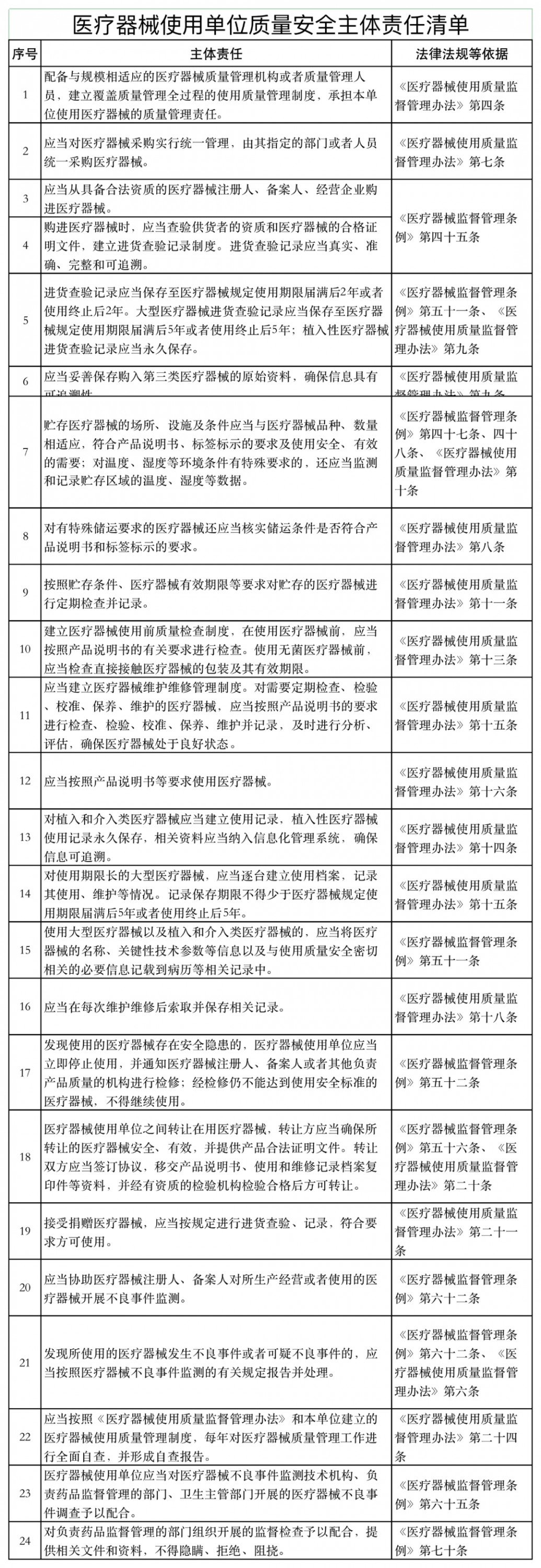
醫(yī)療器械經(jīng)營監(jiān)管大調(diào)整
隨著新版《醫(yī)療器械生產(chǎn)監(jiān)督管理辦法》《醫(yī)療器械經(jīng)營監(jiān)督管理辦法》的落地執(zhí)行,醫(yī)療器械企業(yè)的經(jīng)營和監(jiān)管力度和措施都提升到新的緯度。
國家指出,兩個辦法嚴格貫徹落實“四個最嚴”要求。落實《醫(yī)療器械監(jiān)督管理條例》規(guī)定,全面落實醫(yī)療器械注冊人備案人制度,優(yōu)化行政許可辦理流程,強化監(jiān)督檢查措施,完善監(jiān)督檢查手段,強化企業(yè)主體責任,并進一步加大對違法行為的處罰力度。
《經(jīng)營辦法》一方面進一步強化了企業(yè)質(zhì)量責任。要求企業(yè)從事醫(yī)療器械經(jīng)營,應(yīng)當按照法律法規(guī)和醫(yī)療器械經(jīng)營質(zhì)量管理規(guī)范的要求,建立覆蓋采購、驗收、貯存、銷售、運輸、售后服務(wù)等全過程的質(zhì)量管理制度和質(zhì)量控制措施,并做好相關(guān)記錄,保證經(jīng)營條件和經(jīng)營活動持續(xù)符合要求。
同時,醫(yī)療器械經(jīng)營企業(yè)應(yīng)當建立質(zhì)量管理自查制度,按照醫(yī)療器械經(jīng)營質(zhì)量管理規(guī)范要求進行自查,每年3月31日前向所在地市縣級負責藥品監(jiān)督管理的部門提交上一年度的自查報告。
另一方面更加注重經(jīng)營全過程的質(zhì)量管理。
一是要求醫(yī)療器械經(jīng)營企業(yè)應(yīng)當從具有合法資質(zhì)的醫(yī)療器械注冊人、備案人、經(jīng)營企業(yè)購進醫(yī)療器械,嚴格控制采購和銷售環(huán)節(jié)的資質(zhì)審核,確保醫(yī)療器械的合法流通。
二是重點突出了進貨查驗、銷售環(huán)節(jié)的記錄要求,保證產(chǎn)品的可追溯,并應(yīng)當按照國家有關(guān)規(guī)定執(zhí)行醫(yī)療器械唯一標識制度。
三是強調(diào)了對低溫、冷藏醫(yī)療器械的儲運要求,確保產(chǎn)品運輸質(zhì)量。四是對經(jīng)營企業(yè)的售后服務(wù)提出要求,確保產(chǎn)品的使用安全。
新《經(jīng)營辦法》通過如下措施強化監(jiān)管:一是實施分類分級管理。藥品監(jiān)督管理部門根據(jù)醫(yī)療器械經(jīng)營企業(yè)質(zhì)量管理和所經(jīng)營醫(yī)療器械產(chǎn)品的風險程度,實施分類分級管理并動態(tài)調(diào)整。
二是制定年度檢查計劃。設(shè)區(qū)的市級、縣級負責藥品監(jiān)督管理的部門應(yīng)當制定年度檢查計劃,明確監(jiān)管重點、檢查頻次和覆蓋范圍并組織實施。三是進行延伸檢查。
藥品監(jiān)督管理部門根據(jù)醫(yī)療器械質(zhì)量安全風險防控需要,可以對為醫(yī)療器械經(jīng)營活動提供產(chǎn)品或者服務(wù)的其他相關(guān)單位和個人進行延伸檢查。四是風險會商研判。藥品監(jiān)督管理部門應(yīng)當根據(jù)監(jiān)督檢查、產(chǎn)品抽檢、不良事件監(jiān)測、投訴舉報、行政處罰等情況,定期開展風險會商研判,做好醫(yī)療器械質(zhì)量安全隱患排查和防控處置工作。
信用檔案建設(shè)。設(shè)區(qū)的市級負責藥品監(jiān)督管理的部門應(yīng)當建立并及時更新轄區(qū)內(nèi)醫(yī)療器械經(jīng)營企業(yè)信用檔案。
《生產(chǎn)辦法》方面,在現(xiàn)有的醫(yī)療器械生產(chǎn)許可和備案、監(jiān)督檢查、責任約談等監(jiān)管方式方法的基礎(chǔ)上,從四個方面進一步豐富完善監(jiān)管手段。
一是建立醫(yī)療器械報告制度。規(guī)定年度報告、生產(chǎn)產(chǎn)品品種報告、生產(chǎn)條件變化報告和重新生產(chǎn)報告四種報告形式,以便監(jiān)管部門及時掌握企業(yè)的生產(chǎn)狀況,有針對性地采取監(jiān)管措施。
二是進一步完善監(jiān)督檢查方式方法。明確監(jiān)督檢查、重點檢查、跟蹤檢查、有因檢查和專項檢查等多種監(jiān)督檢查形式,并對有因檢查和跟蹤檢查的內(nèi)容和方式作出具體規(guī)定。
三是細化明確信息公開和責任約談制度。藥品監(jiān)督管理部門依法及時公開醫(yī)療器械生產(chǎn)許可、備案、監(jiān)督檢查、行政處罰等信息,方便公眾查詢,接受社會監(jiān)督。醫(yī)療器械注冊人、備案人、受托生產(chǎn)企業(yè)對存在的醫(yī)療器械質(zhì)量安全風險,未采取有效措施消除的,藥品監(jiān)督管理部門可以對醫(yī)療器械注冊人、備案人、受托生產(chǎn)企業(yè)的法定代表人或者企業(yè)負責人進行責任約談。
委托生產(chǎn)如何開展?
醫(yī)療器械注冊人、備案人委托生產(chǎn)的,應(yīng)當對受托方的質(zhì)量保證能力和風險管理能力進行評估,按照國家藥監(jiān)局制定的委托生產(chǎn)質(zhì)量協(xié)議指南要求,與其簽訂質(zhì)量協(xié)議以及委托協(xié)議,監(jiān)督受托方履行有關(guān)協(xié)議約定的義務(wù);
受托生產(chǎn)企業(yè)應(yīng)當按照法律、法規(guī)、規(guī)章、醫(yī)療器械生產(chǎn)質(zhì)量管理規(guī)范、強制性標準、產(chǎn)品技術(shù)要求、委托生產(chǎn)質(zhì)量協(xié)議等要求組織生產(chǎn),對生產(chǎn)行為負責,并接受醫(yī)療器械注冊人、備案人的監(jiān)督。
受托生產(chǎn)企業(yè)應(yīng)當向原生產(chǎn)許可或者生產(chǎn)備案部門報告增加生產(chǎn)的產(chǎn)品品種情況,并提供委托方、受托生產(chǎn)產(chǎn)品、受托期限等信息;
增加生產(chǎn)產(chǎn)品涉及生產(chǎn)條件變化,可能影響產(chǎn)品安全、有效的,應(yīng)當在增加生產(chǎn)產(chǎn)品30個工作日前向原生產(chǎn)許可部門報告,原生產(chǎn)許可部門應(yīng)當及時開展現(xiàn)場核查。屬于許可事項變化的,應(yīng)當按照規(guī)定辦理相關(guān)許可變更。
醫(yī)療器械注冊人、備案人應(yīng)當負責產(chǎn)品上市放行,建立產(chǎn)品上市放行規(guī)程,明確放行標準、條件,并對醫(yī)療器械生產(chǎn)過程記錄和質(zhì)量檢驗結(jié)果進行審核,符合標準和條件的,經(jīng)授權(quán)的放行人員簽字后方可上市。
委托生產(chǎn)的,醫(yī)療器械注冊人、備案人還應(yīng)當對受托生產(chǎn)企業(yè)的生產(chǎn)放行文件進行審核。
受托生產(chǎn)企業(yè)應(yīng)當建立生產(chǎn)放行規(guī)程,明確生產(chǎn)放行的標準、條件,確認符合標準、條件的,方可出廠。不符合法律、法規(guī)、規(guī)章、強制性標準以及經(jīng)注冊或者備案的產(chǎn)品技術(shù)要求的,不得放行出廠和上市。醫(yī)療器械注冊人、備案人不得委托受托生產(chǎn)企業(yè)進行上市放行。
落實生產(chǎn)產(chǎn)品品種報告制度。醫(yī)療器械生產(chǎn)企業(yè)應(yīng)當向藥品監(jiān)督管理部門報告所生產(chǎn)的產(chǎn)品品種情況。
增加生產(chǎn)產(chǎn)品品種的,應(yīng)當向原生產(chǎn)許可或者生產(chǎn)備案部門報告,涉及委托生產(chǎn)的,還應(yīng)當提供委托方、受托生產(chǎn)產(chǎn)品、受托期限等信息。醫(yī)療器械生產(chǎn)企業(yè)增加生產(chǎn)產(chǎn)品涉及生產(chǎn)條件變化,可能影響產(chǎn)品安全、有效的,應(yīng)當在增加生產(chǎn)產(chǎn)品30個工作日前向原生產(chǎn)許可部門報告,原生產(chǎn)許可部門應(yīng)當及時開展現(xiàn)場核查。屬于許可事項變化的,應(yīng)當按照規(guī)定辦理相關(guān)許可變更。



