9月23日訊 新一輪醫(yī)保目錄調(diào)整進(jìn)行中,據(jù)醫(yī)藥魔方PharmaGo數(shù)據(jù),按照品種數(shù)量維度和獨(dú)家品種維度,哈藥股份、葵花藥業(yè)、現(xiàn)代制藥、華潤(rùn)雙鶴、步長(zhǎng)制藥、豪森醫(yī)藥、恒瑞醫(yī)藥、石藥集團(tuán)等企業(yè)或受益新一輪醫(yī)保目錄調(diào)整。
近日(9月18日),國(guó)家醫(yī)保局公示了《2020年國(guó)家醫(yī)保藥品目錄調(diào)整通過(guò)形式審查的申報(bào)藥品名單》(以下簡(jiǎn)稱《名單》》。
據(jù)賽柏藍(lán)梳理,有728個(gè)藥品通過(guò)了形式審查。此外,目錄內(nèi)需要重新調(diào)整醫(yī)保支付標(biāo)準(zhǔn)、適應(yīng)癥發(fā)生重大改變的談判藥品有23個(gè),也就是說(shuō)此次共有約751個(gè)品種通過(guò)形式審查。
在通知中,國(guó)家醫(yī)保局指出,對(duì)《名單》有意見(jiàn)的相關(guān)主體和個(gè)人可以在9月25日17:00前向其反饋。
根據(jù)新一輪醫(yī)保目錄調(diào)整的工作安排:
1、準(zhǔn)備階段(2020年7-8月);2、申報(bào)階段(2020年8-9月);3、專家評(píng)審階段(2020年9-10月);4、談判和競(jìng)價(jià)階段(2020年10-11月);公布結(jié)果階段(2020年11-12月)
也就是說(shuō)《名單》公示期結(jié)束后,醫(yī)保目錄調(diào)整將進(jìn)入專家評(píng)審階段。
醫(yī)藥魔方的數(shù)據(jù)顯示,哈藥股份、葵花藥業(yè)、現(xiàn)代制藥、華潤(rùn)雙鶴、科倫藥業(yè)、石藥集團(tuán)、廣藥集團(tuán)、輔仁藥業(yè)、修正藥業(yè)、太極集團(tuán)、華潤(rùn)三九等42家藥企通過(guò)國(guó)家醫(yī)保目錄調(diào)整形式審查的藥品數(shù)量較多。
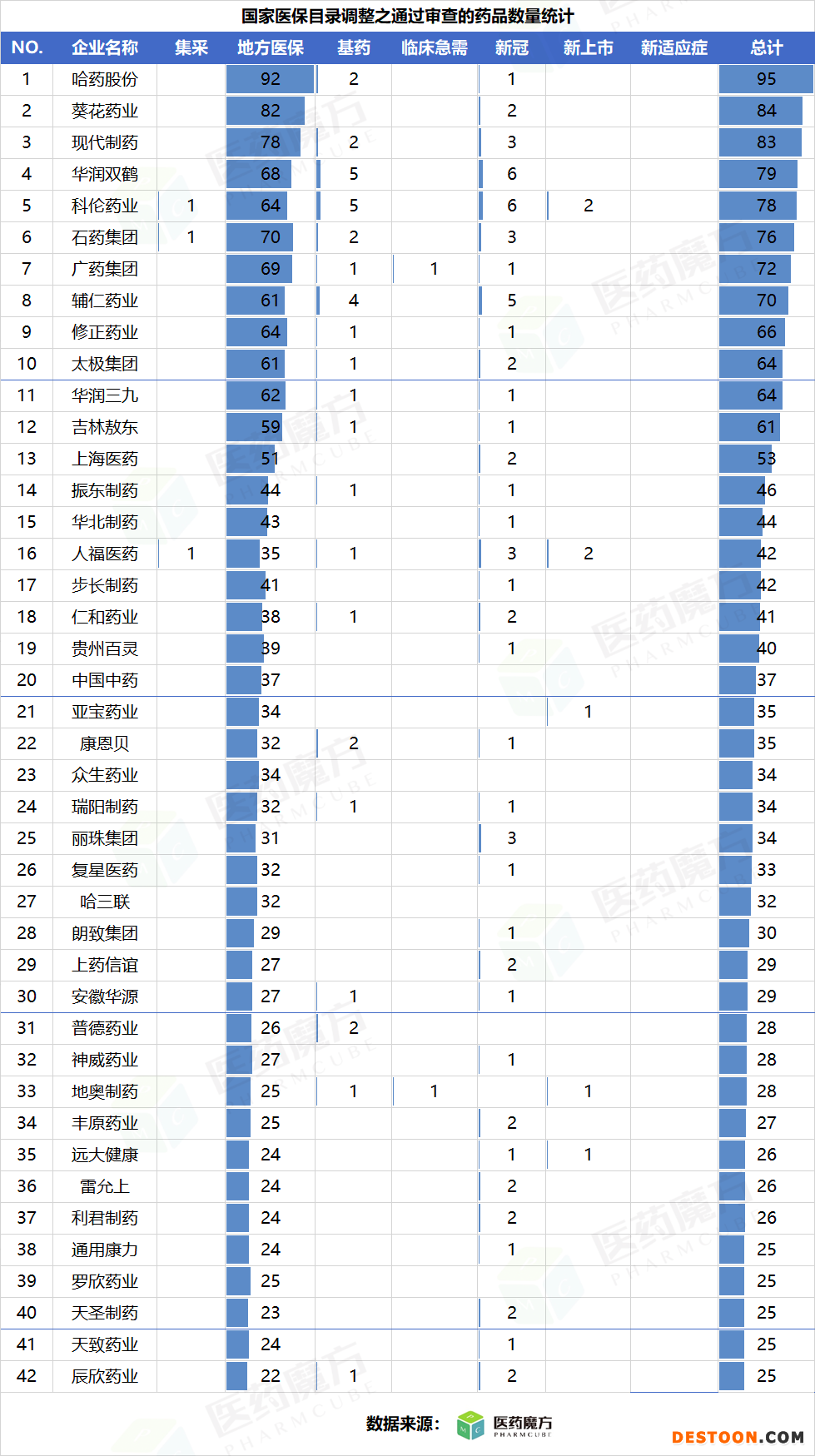
(圖片來(lái)源:醫(yī)藥魔方)
其中,哈藥股份通過(guò)形式審查的藥品數(shù)量達(dá)95個(gè),葵花藥業(yè)通過(guò)形式審查的藥品數(shù)量達(dá)84個(gè),現(xiàn)代制藥通過(guò)形式審查的藥品數(shù)量達(dá)83個(gè),華潤(rùn)雙鶴通過(guò)形式審查的藥品數(shù)量達(dá)79個(gè)。
在這份名單中,通用康力、羅欣藥業(yè)、天圣制藥、天致藥業(yè)、辰欣藥業(yè)5家藥企通過(guò)形式審查的藥品數(shù)量最少,也在25個(gè)。
總的來(lái)看,上述藥企均有望通過(guò)數(shù)量?jī)?yōu)勢(shì),在新一輪國(guó)家醫(yī)保目錄調(diào)整中,謀求不錯(cuò)的結(jié)果。
另外,步長(zhǎng)制藥、豪森醫(yī)藥、北大醫(yī)藥、恒瑞醫(yī)藥、貴州百靈、人福醫(yī)藥、石藥集團(tuán)、地奧制藥等38家藥企通過(guò)國(guó)家醫(yī)保目錄調(diào)整形式審查的獨(dú)家品種數(shù)量較多。
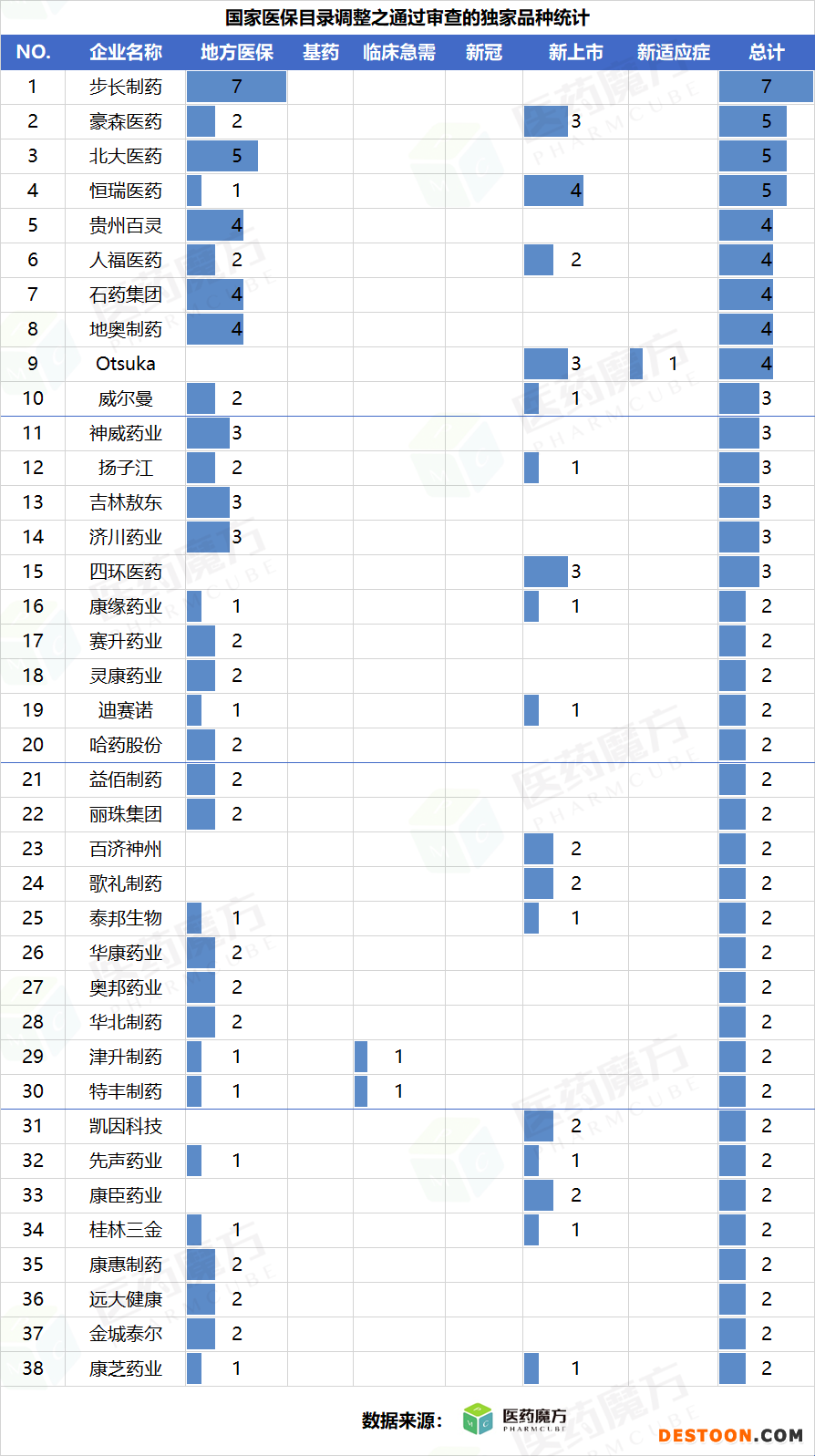
(圖片來(lái)源:醫(yī)藥魔方)
其中,步長(zhǎng)制藥通過(guò)形式審查的藥品數(shù)量達(dá)7個(gè),豪森醫(yī)藥、北大醫(yī)藥、恒瑞醫(yī)藥通過(guò)形式審查的藥品數(shù)量達(dá)5個(gè),貴州百靈、人福醫(yī)藥、石藥集團(tuán)、地奧制藥、Otsuka5家藥企通過(guò)形式審查的藥品數(shù)量為4個(gè)。
至于康緣藥業(yè)、哈藥股份、益佰制藥、麗珠集團(tuán)、百濟(jì)神州、歌禮制藥、華北制藥、先聲藥業(yè)、康辰藥業(yè)、桂林三金、康芝藥業(yè)等企業(yè),雖然通過(guò)形式審查的獨(dú)家品種數(shù)量較少,也在2個(gè)。
醫(yī)保支付標(biāo)準(zhǔn)也是關(guān)注重點(diǎn)
9月1日正式施行的《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》明確,建立完善醫(yī)保目錄動(dòng)態(tài)調(diào)整機(jī)制,原則上國(guó)家醫(yī)保目錄每年調(diào)整一次。
據(jù)梳理,此次通過(guò)形式審查的申報(bào)藥品名單共納入了7類藥品,其中有個(gè)別藥品存在重合。
條件1:納入《新型冠狀病毒肺炎診療方案(試行第七版)》的藥品。
條件2:納入《國(guó)家基本藥物目錄(2018年版)》的藥品。
條件3:納入《臨床急需境外新藥名單(第一批)》《臨床急需境外新藥名單(第二批)》《第一批鼓勵(lì)仿制藥品目錄》《首批鼓勵(lì)研發(fā)申報(bào)兒童藥品清單》或《第三批鼓勵(lì)研發(fā)申報(bào)兒童藥品清單》,且于2020年8月17日前經(jīng)國(guó)家藥監(jiān)部門(mén)批準(zhǔn)上市的藥品。
條件4:第二批國(guó)家組織藥品集中采購(gòu)中選藥品。
條件5:2015年1月1日至2020年8月17日期間,經(jīng)國(guó)家藥監(jiān)部門(mén)批準(zhǔn)上市的新通用名藥品。
條件6:2015年1月1日至2020年8月17日期間,根據(jù)臨床試驗(yàn)結(jié)果向國(guó)家藥監(jiān)部門(mén)補(bǔ)充申請(qǐng)并獲得批準(zhǔn),適應(yīng)癥、功能主治等發(fā)生重大變化的藥品。
條件7:2019年12月31日前,進(jìn)入5個(gè)(含)以上省級(jí)最新版基本醫(yī)保藥品目錄的藥品。其中,主要活性成分被列入《第一批國(guó)家重點(diǎn)監(jiān)控合理用藥藥品目錄(化藥及生物制品)》的除外。
值得注意的是,在上述品種中符合“2019年12月31日前,進(jìn)入5個(gè)(含)以上省級(jí)最新版基本醫(yī)保藥”這一要求的數(shù)量最多,達(dá)493個(gè)。
根據(jù)醫(yī)保調(diào)整的相關(guān)規(guī)定,審查通過(guò)的藥品將進(jìn)入專家評(píng)審階段(要充分考慮到藥學(xué)、藥物經(jīng)濟(jì)、管理、臨床等組的分布),專家評(píng)審階段之后,會(huì)形成新增調(diào)入、直接調(diào)出、可以調(diào)出、調(diào)整限定支付范圍等4方面藥品的建議名單。
此后再經(jīng)過(guò)一系列規(guī)定的流程后,新版醫(yī)保目錄才將正式公布,預(yù)計(jì)新一輪醫(yī)保目錄將于年底面世。
在醫(yī)保目錄調(diào)整的過(guò)程中,相關(guān)藥品醫(yī)保支付標(biāo)準(zhǔn)的確定是除目錄準(zhǔn)入外最受關(guān)注的內(nèi)容。
根據(jù)《基本醫(yī)療保險(xiǎn)用藥管理暫行辦法》第十二條規(guī)定:
建立《藥品目錄》準(zhǔn)入與醫(yī)保藥品支付標(biāo)準(zhǔn)銜接機(jī)制。除中藥飲片外,原則上新納入《藥品目錄》的藥品同步確定支付標(biāo)準(zhǔn)。
獨(dú)家藥品通過(guò)準(zhǔn)入談判的方式確定支付標(biāo)準(zhǔn)。
非獨(dú)家藥品中,國(guó)家組織藥品集中采購(gòu)中選藥品,按照集中采購(gòu)有關(guān)規(guī)定確定支付標(biāo)準(zhǔn);其他非獨(dú)家藥品根據(jù)準(zhǔn)入競(jìng)價(jià)等方式確定支付標(biāo)準(zhǔn)。
執(zhí)行政府定價(jià)的麻醉藥品和第一類精神藥品,支付標(biāo)準(zhǔn)按照政府定價(jià)確定。
必須要說(shuō)的是,隨著新版醫(yī)保目錄的公布,相關(guān)藥企到底是喜是憂,我們只能在正式目錄公布后才能獲得答案。



 110102000668(1)號(hào)
110102000668(1)號(hào)